Alors que le point de fusion de l'oxygène est de \( -218,8 °C \) , le diamant ne fond pas du tout dans des conditions atmosphériques normales. Au contraire, il ne se sublime qu'à la température torride de \( 3 700 °C \) . Quelle est la cause de ces différences de propriétés physiques ? Tout est lié aux liaisons intermoléculaires et intramoléculaires.
- Ce résumé de cours porte sur les liaisons intermoléculaires.
- Tout d'abord, nous allons définir la molécule et la polarité.
- Ensuite, nous expliquerons les molécules polaires et apolaires.
- Puis, nous examinerons la liaison intramoléculaire et liaison covalente.
- Enfin, nous verrons la force de London et des exemples des forces intermoléculaires.
Qu'est-ce qu'une molécule ?
Une molécule est la plus petite portion d'une substance qui conserve ses propriétés chimiques et physiques. Chaque molécule est un système composé d'un ensemble d'atomes organisés et liés entre eux.
Ces atomes peuvent être du même élément ou d'éléments différents, auquel cas, ils sont appelés composés.
Polarité : définition
La polarité est le résultat de la répartition inégale des charges partielles entre les différents atomes d'un composé ou molécule.
Molécules polaires
Les molécules polaires sont des molécules qui ne partagent pas uniformément les électrons à travers la liaison covalente et qui présentent des dipôles sur les atomes impliqués.
Les dipôles sont de petites charges partielles qui se produisent en raison du partage inégal des électrons.
Les liaisons covalentes polaires se produisent lorsque deux atomes ont une liaison covalente, mais ont une électronégativité légèrement différente.
L'atome le plus électronégatif rapproche alors les électrons de la liaison, ce qui lui confère un dipôle négatif. L'autre atome obtient à son tour un dipôle positif. Cela crée une molécule polaire dont le partage des électrons est inégal.
Molécule apolaire
Une molécule apolaire est une molécule qui ne possède aucune charge électrique ou charge partielle.
Les molécules apolaires sont composées d'atomes qui ont une valeur d'électronégativité similaire. Lorsque deux atomes d'électronégativité similaire partagent des électrons dans une liaison covalente, ils sont attirés vers l'un ou l'autre atome de manière égale. Il y a donc une répartition égale de la charge et la molécule entière est neutre, et donc apolaire. Deux exemples importants de molécules apolaires sont l'oxygène \( O=O \) et le dioxyde de carbone \( O=C=O \) .
Qu'est-ce qu'une liaison intramoléculaire ?
La liaison intramoléculaire est la liaison qui relie les atomes entre eux et qui permet de former des composés. Il existe \( 3 \) types de liaisons intramoléculaires : covalentes, ioniques et métalliques.
Liaison covalente
La liaison covalente est la liaison dans laquelle une ou plusieurs paires d'électrons sont partagées par deux atomes.
Les composés moléculaires désignent des espèces liées par covalence, généralement de faible masse moléculaire.
Les composés macromoléculaires sont des composés de masse moléculaire élevée, liés par covalence et linéaires, ramifiés ou réticulés.
Liaison ionique
Une liaison ionique est une attraction électrostatique entre des ions de charge opposée, formée lorsqu'un atome transfère des électrons à un autre.
Le(s) électron(s) impliqué(s) dans la liaison ionique est (sont) transféré(s) de l'atome le moins électronégatif vers l'atome le plus électronégatif, formant ainsi des ions.
Liaison métallique
La liaison métallique est une liaison résultant de l'attraction entre des ions positifs et des électrons mobiles qui l'entourent.
Qu'est-ce qu'une liaison intermoléculaire ?
Les forces intermoléculaires sont des forces entre les molécules.
Ces forces sont plus faibles que les forces intramoléculaires, et leur rupture ne nécessite pas autant d'énergie.
Une molécule subira différents types de forces intermoléculaires en fonction de sa polarité. Examinons-les chacune à leur tour.
Forces de Van der Waals
Les forces de Van der Waals sont le type le plus faible de force intermoléculaire. Elles portent de nombreux noms différents - par exemple, forces de London, forces dipolaires induites ou forces de dispersion. On les trouve dans toutes les molécules, y compris les molécules apolaires.
Les forces de Van der Waals sont un type de force intermoléculaire que l'on retrouve entre toutes les molécules, en raison des dipôles temporaires qui sont causés par le mouvement aléatoire des électrons.
La force de Van der Waals augmente avec la taille de la molécule. Cela s'explique par le fait que les grosses molécules ont plus d'électrons. Cela crée un dipôle temporaire plus fort.
Force de London
La force de London est classée dans la catégorie des forces de van der Waal. Elle est la plus faible des forces intermoléculaires et existe entre tous les types de molécules, qu'elles soient ioniques ou covalentes, polaires ou apolaires. Plus une molécule possède d'électrons, plus les forces de London sont fortes.
Forces dipôle-dipôle permanentes
Les molécules dont les moments dipolaires ne s'annulent pas mutuellement présentent ce que l'on appelle un dipôle permanent. Une partie de la molécule est partiellement chargée négativement, tandis qu'une autre est partiellement chargée positivement. Les dipôles de charge opposée dans des molécules voisines s'attirent mutuellement et les dipôles de charge similaire se repoussent.
Les forces dipôle-dipôle permanentes sont un type de force intermoléculaire que l'on retrouve entre deux molécules possédant des dipôles permanents.
Qu'est-ce qu'une liaison hydrogène ?
Une liaison hydrogène est l'attraction électrostatique entre un atome d'hydrogène lié de manière covalente à un atome extrêmement électronégatif, et un autre atome électronégatif avec une paire d'électrons solitaires.
Tous les éléments ne peuvent pas former des liaisons hydrogène. En fait, seuls trois le peuvent : le fluor, l'oxygène et l'azote. Pour former une liaison hydrogène, il faut un atome d'hydrogène lié à un atome très électronégatif qui possède une paire d'électrons solitaires et seuls ces trois éléments sont suffisamment électronégatifs.
Les liaisons hydrogène sont beaucoup plus fortes que les forces dipôle-dipôle permanentes et les forces de dispersion. Elles nécessitent plus d'énergie pour être surmontées.
| Force intermoléculaire | Se produit entre… | Force relative |
| L'attraction dipôle-dipôle | Des ions partiellement chargés de manière opposée | Forte |
| Liaison hydrogène | L'atome \( H \) et l'atome \( O, N \) ou l'atome \( F \) | La plus forte des attractions dipôle-dipôle. |
| Attraction de la force de London | Dipôles temporaires ou induits | La plus faible |
Tableau de la force relative des forces d'attraction intermoléculaires.
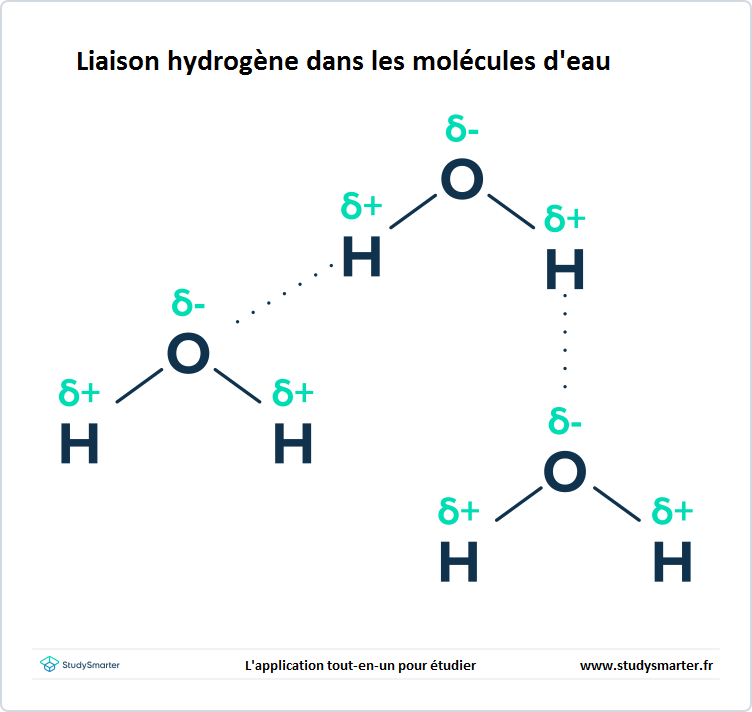
Fig.1- Liaison hydrogène dans les molécules d'eau.
Exemples de forces intermoléculaires
Examinons quelques molécules courantes et prédisons les forces intermoléculaires qu'elles subissent.
Le monoxyde de carbone, \( CO \) , est une molécule polaire et présente donc des forces dipôle-dipôle permanentes et des forces de van der Waals entre les molécules. En revanche, le dioxyde de carbone, \( CO_2 \) , ne subit que des forces de van der Waals. Bien qu'il contienne des liaisons polaires, c'est une molécule symétrique et les moments dipolaires s'annulent.
 Fig. 2- La polarité des liaisons dans le monoxyde de carbone, à gauche, et le dioxyde de carbone, à droite.
Fig. 2- La polarité des liaisons dans le monoxyde de carbone, à gauche, et le dioxyde de carbone, à droite.
Le méthane, \( CH_4 \) , et l'ammoniac, \( NH_3 \) , sont des molécules de taille similaire. Elles subissent donc des forces de van der Waals de force similaire, que nous connaissons également sous le nom de forces de dispersion. Cependant, le point d'ébullition de l'ammoniac est beaucoup plus élevé que celui du méthane. Cela s'explique par le fait que les molécules d'ammoniac peuvent se lier à l'hydrogène, ce qui n'est pas le cas des molécules de méthane. En fait, le méthane n'a même pas de forces dipôle-dipôle permanentes, car ses liaisons sont toutes apolaires. Les liaisons hydrogène sont beaucoup plus fortes que les forces de van der Waals, et il faut donc beaucoup plus d'énergie pour les surmonter et faire bouillir la substance.
 Fig. 3- Le méthane est une molécule non polaire. En revanche, l'ammoniac est une molécule polaire et forme des liaisons hydrogène entre les molécules.
Fig. 3- Le méthane est une molécule non polaire. En revanche, l'ammoniac est une molécule polaire et forme des liaisons hydrogène entre les molécules.
Liaisons intermoléculaires - Points clés
- Les forces intramoléculaires sont des forces au sein des molécules, tandis que les forces intermoléculaires sont des forces entre les molécules. Les forces intramoléculaires sont beaucoup plus fortes que les forces intermoléculaires.
- La polarité détermine le type de forces intermoléculaires entre les molécules.
- Les molécules polaires se produisent lorsqu'il existe une différence d'électronégativité entre les atomes liés.
- Les molécules apolaires se produisent lorsque les électrons sont partagés de manière égale entre les atomes.
- Il existe \( 3 \) types de liaisons intramoléculaires : covalentes, ioniques et métalliques.
- Les forces de Van der Waals, également appelées forces de London ou forces de dispersion, existent entre toutes les molécules et sont causées par des dipôles temporaires. Ces dipôles temporaires sont dus au mouvement aléatoire des électrons et créent des dipôles induits dans les molécules voisines.
- Les liaisons hydrogène sont le type de force intermoléculaire le plus puissant. On les trouve entre les molécules contenant un atome de fluor, d'oxygène ou d'azote, lié à un atome d'hydrogène.










