Et si je te disais que la plupart des choses dans la nature existent sous cette forme tout le temps (au moins au niveau microscopique) - comment ces éléments fonctionnent-ils dans un tel état d'enchevêtrement ?
Dans cet article, nous allons apprendre ce qu'est un polymère amorphe, et quelles sont ses propriétés et caractéristiques, aux côtés de son rival, le fameux polymère cristallin. Allons-y !
- Polymères amorphes Définition : définir ce que sont les polymères amorphes en désintégrant le mot lui-même et en abordant chaque section.
- Propriétés des polymères amorphes : discuter des différentes propriétés et caractéristiques.
- Points de fusion des polymères amorphes : focus approfondi sur le point de fusion des polymères amorphes.
- Exemples de polymères amor phes : fournir quelques exemples sur le sujet en question.
- Différence entre amorphe et cristallin : expliquer les différences entre les polymères amorphes et cristallins.
Définition des polymères amorphes :
Avant de sauter dans les détails techniques de ce que sont les polymères amorphes, décomposons ce mot à l'aspect effrayant et essayons de comprendre ce que chaque élément représente !
Tout d'abord, que signifie le mot "amorphe" ?
Amorphe signifie l'état d'une substance qui, lorsqu'elle est bombardée de rayons X, ne forme pas de figure de diffraction. Les figures de diffraction régulièrement ordonnées qui ont tendance à être associées aux réseaux cristallins. Par conséquent, toutes les substances dont les molécules ne sont pas constituées de structures ordonnées et périodiques, typiques des cristaux, sont dites amorphes .
En résumé, dans un solide amorphe, il n'y a pas d'ordre dans la position des atomes ou des molécules qui le constituent.
Mais comment se forment les solides amorphes ? Ils peuvent être obtenus en refroidissant un liquide en dessous de son point de solidification, ce qui réduit la mobilité d'une molécule : le corps obtient un niveau élevé de viscosité qui rend son état similaire à celui d'un solide.
Viscosité des polymères amorphes
Comme mentionné ci-dessus, un solide amorphe se forme lorsque le processus de cristallisation est très lent, en raison de la viscosité élevée de la substance. Qu'est-ce que la viscosité?
Laviscosité est la résistance au mouvement des particules due aux forces intermoléculaires (friction interne). La viscosité est indiquée par la vitesse ou la mobilité des particules dans un liquide.
Ainsi, lors du passage de l'état liquide à l'état solide (processus appelé solidification), les substances à forte viscosité deviennent d'abord un solide amorphe, puis un solide cristallin.
Laviscosité diminue avec l'augmentation de la température. On obtient généralement un solide amorphe si la substance fondue a une vitesse de refroidissement très élevée.
Prenons en considération la silice (SiO2) :
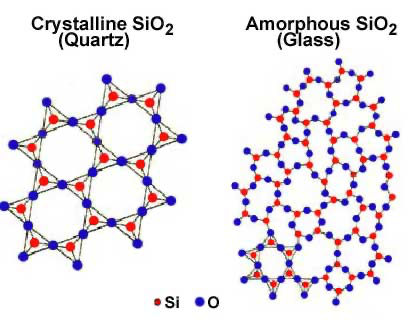
La silice est une molécule covalente polaire qui constitue le réseau d'un solide cristallin. Par conséquent, elle possède une structure de particules bien organisée. Comment se fait-il alors qu'elle prenne un état amorphe ?
Le solide a la capacité de se transformer en liquide à des températures élevées. Ce qui se passe ici, c'est que la structure cristalline de la silice est détruite au cours d'un processus appelé fusion, ce qui permet aux ions de migrer librement.
Lorsque la forme fondue refroidit, la viscosité augmente, ce qui empêche le cristal de se reformer. Le matériau revient ensuite à l'état solide après avoir refroidi, mais la structure interne est différente, elle est devenue erratique.
Parmi les quelques substances connues pour atteindre un état amorphe, la plus importante est le verre, l'état vitreux de la matière !
Le verre n'est pas un liquide qui se déplace lentement. C'est en fait un très bon solide que l'on place dans la catégorie des amorphes, car il n'a pas la structure moléculaire ordonnée des vrais solides, mais il est trop rigide pour être considéré comme un liquide en raison de sa structure irrégulière.
 Structure amorphe du verre : https://www.e-education.psu.edu/matse81/node/2154
Structure amorphe du verre : https://www.e-education.psu.edu/matse81/node/2154
Il s'ensuit rapidement que les éléments mentionnés ci-dessus subissent un processus appelé "amorphisation", processus que je définirai ci-dessous.
L'amorphisation est la modification de l'état cristallin en un état amorphe. Cette amorphisation est souvent réalisée par différents moyens (par exemple, bombardement avec des électrons ou des ions de haute énergie, irradiation avec de courtes impulsions laser et réactions en phase solide).
Un autre type d'amorphisation est appelé amorphisation induite par la pression.
Lorsqu'un solide cristallin est comprimé au-delà de sa plage de stabilité normale à une température bien inférieure au point de fusion du matériau, les changements de phase cristalline prévus ne peuvent pas commencer ou se terminer. Ce phénomène est connu sous le nom d'amorphisation induite par la pression (PIA).
Pour en revenir à notre mot-clé principal, le polymère amorphe, nous pouvons maintenant apprendre ce que signifie le mot "polymère".
Un polymère est une grosse molécule qui se présente sous la forme d'une longue chaîne avec plusieurs branches qui peuvent être reliées entre elles.
Une façon simple et rapide de mémoriser ce terme : En latin, le mot "poly" signifie beaucoup tandis que le mot "mer" signifie unité. Par conséquent, le terme polymère, décomposé, signifie en réalité beaucoup d'unités.
Les origines des polymères proviennent des monomères, des molécules simples qui peuvent être agrégées en groupes de deux, trois, quatre ou plus (et sont donc appelées dimères, trimères, tétramères, etc.) ou en centaines(polymères).
La cellulose, qui est composée de nombreuses unités de sucre, est un exemple de polymère naturel de poids élevé. Le caoutchouc et les plastiques, la laine et l'amidon sont également des exemples d'autres polymères !
On peut maintenant classer les polymères en deux grandes sous-catégories :
 Polymères amorphes ou cristallins : https://pediaa.com/difference-between-amorphous-and-crystalline-polymers/
Polymères amorphes ou cristallins : https://pediaa.com/difference-between-amorphous-and-crystalline-polymers/
Alors, comment tout cela s'articule-t-il ? Découvrons-le !
Comme nous l'avons appris plus haut, amorphe signifie un solide qui manque d'ordre dans la position des atomes ou des molécules qui le constituent. Les polymères peuvent se présenter sous la forme d'un très grand nombre de molécules liées entre elles en une seule unité macromoléculaire. Si l'on ajoute ces deux définitions, on obtient :
Lespolymères amorphes sont des solides dont les chaînes moléculaires sont disposées de manière désordonnée dans l'espace !
Lespolymères amorphes sont constitués de zones amorphes où les molécules sont organisées de façon aléatoire. Tu vois cette ligne sinueuse aléatoire dans l'image ci-dessus ? C'est probablement la façon la plus précise de représenter un polymère amorphe.
Propriétés des polymères amorphes :
Les polymères amorphes ont généralement des propriétés anisotropes, car il n'y a pas de direction particulière dans l'arrangement des particules, ce qui se traduit par :
- Température de fusion inexacte : La température de fusion se produit sur une large plage de températures puisque la fusion dépend d'une diminution de la viscosité plutôt que de la rupture des liaisons intramoléculaires.
- Température de solidification inexacte : La température de solidification se produit sur une large plage de températures car la solidification dépend d'une augmentation de la viscosité plutôt que de la rupture des liaisons intramoléculaires.
- Ils possèdent des caractéristiques élastiques lorsque la température augmente.
- Indice de réfraction élevé : Les verres ont un indice de réfraction élevé, c'est pourquoi ils sont transparents. La structure désordonnée typique des liquides confère aux solides la propriété d'un indice de réfraction élevé, c'est-à-dire la transparence.
- Ils ont tendance à être vitreux, durs et cassants .
- Transparents.
- Faible densité.
- Mauvaise résistance à lafatigue et à l'usure.
L'indice de réfraction indique le rapport entre la vitesse à laquelle un rayon traverse un milieu spécifique et la vitesse à laquelle il traverse un second milieu.
Point de fusion des polymères amorphes :
Les polymères amorphes ont une température de transition vitreuse, ou Tg, plutôt qu'un point de fusion.
La température à laquelle le polymère devient mou en raison d'un mouvement moléculaire coordonné à longue portée est connue sous le nom de température de transition vitreuse (Tg).
Pense à ceci : as-tu déjà laissé un récipient en plastique ou tout autre objet en plastique à l'extérieur en hiver et constaté qu'il se cassait ou se fissurait plus facilement qu'en été ? Ce que tu as expérimenté dans ce cas, c'est le phénomène connu sous le nom de transition vitreuse. Cette transition ne se produit que dans les polymères, et c'est l'une des caractéristiques qui les rendent uniques.
La transition vitreuse est beaucoup plus compliquée qu'il n'y paraît. Il existe une certaine température (différente pour chaque polymère) appelée température de transition vitreuse, ou Tg , qui joue un rôle important dans son processus. En effet ,
lorsque le polymère est refroidi en dessous de cette température, il devient rigide et cassant comme du verre.
Il peut être facile de supposer que la transition vitreuse est comparable à la fusion. Cependant, ce n'est pas le cas. La fusion est une transition qui se produit dans les polymères recristallisés, et non dans les polymères amorphes. De plus, la fusion se produit lorsque les chaînes de polymères passent de leur structure cristalline à un état de désordre liquide. La transition vitreuse est une transition qui se produit dans les polymères amorphes !
Exemples de polymères amorphes :
Leverre, le propylène et laglace sont des exemples de solides amorphes!
- Leverre est un solide amorphe ayant la structure d'un liquide, qui prend la forme du récipient qui le contient. C'est à la base un produit qui, après avoir été fondu, est refroidi à grande vitesse, ce qui permet la formation de cristaux.
- Lepropylène (C3H6) est une matière thermoplastique obtenue par polymérisation d'un dérivé d'hydrocarbure, le propylène.
- Laglace a une densité inférieure à celle de l'eau liquide. Les réseaux cristallins de glace qui se forment lors de la congélation sont généralement très différents les uns des autres, c'est pourquoi on considère qu'elle appartient à la liste des polymères amorphes.
Différence entre amorphe et cristallin :
Avant d'aborder la différence, comprenons très rapidement ce que sont les polymères cristallins :
Les polymèrescristallins sont des polymères dont certaines parties ont cristallisé dans un ordre précis, permettant la formation d'une unité solide organisée.
Bien qu'il soit possible de créer une structure 100% amorphe, il est impossible de créer une structure 100% cristalline car les polymères cristallins contiennent toujours un nombre décent de polymères amorphes.
Maintenant que la définition est posée, abordons les principales différences :
| Polymères amorphes | Polymères cristallins |
| Molécules non uniformément emballées. | Molécules uniformément tassées. |
| Faible densité. | Haute densité. |
| Transparents. | Opaque/Translucide. |
| Faible rétrécissement. | Rétrécissement élevé. |
| Point de fusion élevé. | Point de fusion bas. |
Polymère amorphe - Principaux enseignements
- Dans un solide amorphe, il n'y a pas d'ordre dans la position des atomes ou des molécules qui le constituent.
- Laviscosité est la résistance au mouvement des particules due aux forces intermoléculaires (friction interne). La viscosité est indiquée par la vitesse de mobilité des particules d'un liquide.
- Un polymère signifie une grosse molécule qui se présente comme une longue chaîne avec plusieurs branches qui peuvent être reliées entre elles.
- Lespolymères amorphes sont des solides dont les chaînes moléculaires sont disposées de façon désordonnée dans l'espace !
- Les polymèrescristallins sont des polymères dont certaines parties se sont cristallisées dans un ordre précis, permettant la formation d'une unité solide organisée.
- Bien qu'il soit possible de créer une structure 100 % amorphe, il est impossible de créer une structure 100 % cristalline car les polymères cristallins contiennent toujours un nombre décent de polymères amorphes.
- Les polymères amorphes ont une température de transition vitreuse, ou Tg, plutôt qu'un point de fusion.










