Nous allons explorer la signification et l'explication de la théorie VSEPR et qui l'a proposée, ainsi que nous plonger dans les applications de la théorie avec des exemples et leurs hypothèses.
Les principaux points qui seront abordés sont les structures de Lewis et les géométries moléculaires basées sur des géométries à deux, trois, quatre, cinq et six électrons, ainsi que certaines hypothèses et incohérences de la théorie, comme le comportement des paires non liées.
- Cette explication porte sur la théorie VSEPR en chimie.
- Tout d'abord, nous verrons qui a proposé la théorie VSEPR et ce que signifie la théorie VSEPR.
- Nous essaierons ensuite d'étudier les structures de Lewis.
- Nous présenterons les différentes géométries des molécules basées sur les géométries à deux, trois, quatre, cinq et six électrons.
- Tu seras capable de nommer et de décrire les formes des molécules en fonction de leurs électrons de valence.
- Enfin, nous verrons un tableau VSEPR représentant les géométries des molécules.
Théorie VSEPR : cours
Les molécules ne sont pas disposées au hasard. En fait, elles prennent toujours des formes spécifiques. Nous appelons la forme d'une molécule sa géométrie, et la géométrie dépend des électrons de valence d'une molécule. Plus précisément, elle dépend du nombre de doublets d'électrons liants et non-liants. Tout cela peut être résumé en un modèle pratique connu sous le nom de théorie VSEPR.
Règle de Gillespie
La théorie VSEPR n'a pas été proposée par un seul chercheur. Il s'agit plutôt d'une idée à laquelle de nombreux scientifiques de renom ont contribué. Elle a d'abord été proposée par Sidgwick et Powell en 1940, puis développée en un domaine complet de la chimie théorique par Ronald Gillespie et Sir Ronald Nyholm en 1957.
La règle de Gillespie est une méthode utilisée pour prévoir la structure des molécules à l'aide de la théorie VSEPR.
C'est quoi la théorie VSEPR ?
La théorie VSEPR a ensuite été testée par de nombreuses méthodes différentes, avant d'être confirmée. Elle a réellement montré comment une théorie mathématique peut expliquer la forme des molécules, l'interaction et le comportement des molécules et des composés entre eux.
La théorie VSEPR signifie théorie de la répulsion des paires d'électrons de la couche de valence. Il s'agit d'un ensemble de règles utilisées en chimie pour prédire la géométrie d'une molécule. Elle est basée sur le nombre et la disposition des électrons de valence de la molécule.
La théorie VSEPR repose sur deux principes clés.
- Les doublets d'électrons se repoussent mutuellement. Pour cette raison, les paires d'électrons autour d'un atome central essaieront de prendre des positions aussi éloignées que possible les unes des autres.
- Les doublets d'électrons non-liants repoussent davantage les autres électrons que les doublets liants. Pour cette raison, la présence de doublets d'électrons non-liants rapprochera deux doublets d'électrons liants, modifiant ainsi la géométrie de la molécule.
Examinons plus en détail les deux idées ci-dessus.
Répulsion des paires d'électrons
Tout d'abord, les paires d'électrons se repoussent mutuellement. Toutes les paires d'électrons sont chargées négativement, et les charges similaires ne s'entendent pas : elles se repoussent toujours. Par conséquent, les paires d'électrons autour d'un atome central essaient de rester aussi éloignées que possible les unes des autres. Cela implique généralement un espacement égal autour de l'atome central. Pour cette raison, les molécules comportant un certain nombre de paires d'électrons ont une certaine forme et certains angles entre leurs liaisons. En fait, toutes les molécules ayant le même nombre de paires d'électrons ont la même forme de base.
Par exemple, supposons qu'un atome central ne possède que deux paires d'électrons, toutes deux impliquées dans des liaisons covalentes simples. Les paires d'électrons sont aussi éloignées l'une de l'autre que possible lorsqu'elles se trouvent sur les côtés opposés de l'atome. Cela donne une molécule linéaire, avec un angle de \( 180° \) entre les paires de liaisons. Ne t'inquiète pas, nous verrons dans quelques instants le nom des molécules de formes différentes.
Méthode VSEPR
La méthode VSEPR s'applique à des molécules de types \(AX_nE_m \)
- \( A \) représente l'atome central.
- \( X_n \) représente le nombre n d'atomes X lies à \( A \) .
- \(E_m \) représente le nombre m de paires d'électrons libres (doublets non liants) autour de \( A \) .
Les hypothèses clés que nous devons prendre en compte sont les différences entre les liaisons et les espèces de domaines électroniques.
- Premièrement, une double liaison se comportera différemment d'une liaison simple, mais la théorie la considérera comme un domaine électronique unique.
- Deuxièmement, nous devons tenir compte du fait qu'une paire d'électrons non liée aura une plus grande répulsion qu'une paire d'électrons liée.
Souvent, dans les géométries moléculaires, la forme sera différente, notamment les valeurs des angles, car les paires non liées exerceront une plus grande répulsion que les électrons liés. Cela peut déformer la forme en différentes conformations.
Lewis : VSEPR
Les structures de Lewis mettent en évidence la présence d'électrons liés et de paires d'électrons non liées. Faire la distinction entre ces espèces par rapport à un atome spécifique permet de créer des formes basées sur le VSEPR.
Dans une structure de Lewis, une paire d'électrons peut être représentée soit par deux points, soit par une ligne.
Une paire d'électrons dans la couche la plus externe est souvent appelée paire d'électrons non liées.
Tu trouveras ci-dessous un exemple du passage des liaisons créées par leurs structures de Lewis :
 Fig.1- La distinction entre la paire de liaisons et la paire d'électrons solitaires est illustrée dans les structures de Lewis
Fig.1- La distinction entre la paire de liaisons et la paire d'électrons solitaires est illustrée dans les structures de Lewis
Pense à la forme 3D qu'adoptera la molécule. Comme il s'agit d'une molécule diatomique, nous pouvons supposer que la forme la plus probable qu'elle adoptera sera une géométrie linéaire. Mais qu'en est-il des molécules plus complexes ?
Dans la section suivante, nous allons voir comment la théorie VSEPR se base sur la répulsion des paires d'électrons, comme expliqué ci-dessus.
Dans l'exemple ci-dessus de la molécule diatomique \( F_2 \) , nous pouvons voir qu'il existe une liaison. Les paires non liées individuelles veulent s'écarter le plus possible pour créer une géométrie linéaire. Nous pouvons affirmer que la géométrie linéaire est atteinte (puisque nous savons que l'angle n'est pas courbe), la forme moléculaire a donc un angle de \( 180° \) .
VSEPR : Angles
Nous savons maintenant que les molécules ayant le même nombre de paires d'électrons ont toutes la même forme de base. Mais en ce qui concerne la géométrie et la répulsion des paires d'électrons, toutes les paires d'électrons ne sont pas égales. Cela modifie légèrement la forme de la molécule. En effet, les doublets non-liants repoussent les autres doublets d'électrons beaucoup plus fortement que les doublets liants. Si les doublets non-liants sont présents, ils rapprochent les doublets liants. Cela diminue l'angle entre les doublets liants et modifie la forme de la molécule.
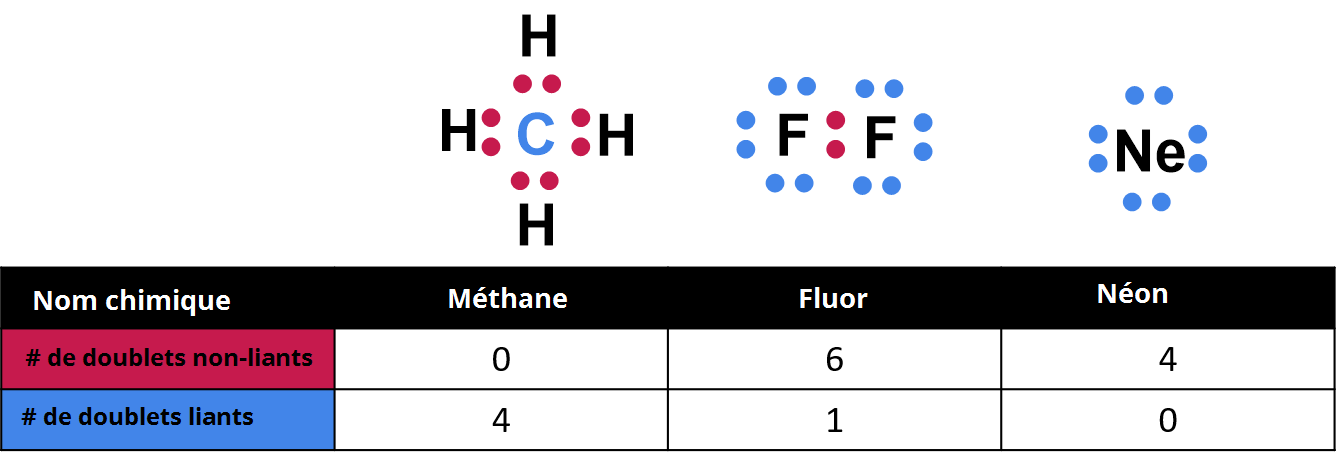
Fig.2- Exemples de molécules avec des paires d'électrons liantes et non liantes
1.
Par exemple, une molécule comportant quatre paires d'électrons autour d'un atome central est toujours basée sur une forme tétraédrique. Si les quatre paires d'électrons sont des paires liées, l'angle entre les liaisons est d'environ \( 109,5° \) . Mais si tu échanges l'une des paires liées contre une paire non liée, l'angle entre les trois liaisons restantes diminue jusqu'à \( 107,0° \) , et la forme change légèrement, devenant une pyramide trigonale. Si l'on échange une autre paire de liaisons, l'angle diminue à \( 104,5° \) , ce qui donne à la molécule une forme en V.
Les liaisons covalentes doubles et triples contiennent respectivement deux et trois paires d'électrons liées. Dans la théorie VSEPR, nous considérons qu'elles forment une "super paire". Les molécules avec ces "super paires" ont la même géométrie que les molécules avec des paires d'électrons liées standards. Nous en verrons quelques exemples plus tard.
Maintenant que nous avons examiné les principes fondamentaux de la théorie VSPER, passons aux géométries des molécules elles-mêmes.
Géométrie des molécules : VSEPR
La théorie de la répulsion des paires d'électrons de la couche de Valence, ou VSEPR, est un modèle utilisé en chimie pour prédire la géométrie des molécules.
Il faut savoir que les électrons ont tendance à se déplacer par paires. En effet, les orbitales, qui sont des régions de l'espace où se trouvent les électrons dans \( 95 \% \) des cas, ne peuvent contenir que deux électrons au maximum. Les électrons étant des particules chargées, les paires d'électrons se repoussent mutuellement et essaient de s'éloigner le plus possible les unes des autres. La couche externe d'électrons d'un atome est appelée couche de valence. Comme les électrons de valence d'une molécule covalente simple sont les électrons liés, la répulsion des paires d'électrons détermine la position des liaisons. Cela détermine la géométrie de la molécule.
VSEPR affirme que les paires d'électrons se repoussent toutes et tentent de prendre des positions aussi éloignées que possible les unes des autres, afin de minimiser la répulsion. Il utilise simplement notre connaissance du comportement des électrons pour prédire la forme des composés covalents simples.
Consulte la rubrique Liaison covalente et liaison dative pour te rappeler comment les atomes partagent les électrons afin d'obtenir des configurations électroniques stables.
Nous avons appris que la théorie VSEPR utilise le nombre et la disposition des électrons de valence pour prédire la géométrie d'une molécule. Nous allons maintenant nous concentrer sur les différentes géométries causées par un nombre variable de paires d'électrons, en commençant par les molécules avec seulement deux paires et en allant jusqu'à celles qui en ont six. Nous commencerons par la forme de base de chaque molécule, qui se produit lorsque toutes les paires d'électrons sont des doublets liants, avant d'explorer l'effet de l'échange de certaines d'entre elles contre des doublets non-liants.
Théorie VSEPR sur les domaines à deux et trois électrons
Le schéma ci-dessous montre les géométries des molécules avec deux ou trois atomes liés à un atome central.
 Fig.3- On peut voir ici une représentation graphique des géométries moléculaires linéaires et trigonales planes, telles que basées sur VSEPR.
Fig.3- On peut voir ici une représentation graphique des géométries moléculaires linéaires et trigonales planes, telles que basées sur VSEPR.
Linéaire
Les molécules comportant seulement deux paires d'électrons ont une forme linéaire. Les deux paires d'électrons, qu'elles soient liées ou non liées, se positionnent aussi loin que possible l'une de l'autre. Cela signifie qu'elles se retrouvent directement opposées l'une à l'autre. L'angle entre les deux liaisons est donc de \( 180 ^o \) .
Ils sont constitués de deux atomes reliés à un atome central par des liaisons covalentes simples ou doubles. Dans les deux cas, l'angle de liaison est de \( 180° \) .
La représentation de Lewis de la molécule de chlorure de béryllium \( BeCl_2 \) est :
 Fig.4- Le chlorure de béryllium, une molécule linéaire.
Fig.4- Le chlorure de béryllium, une molécule linéaire.
$$ X= 2 $$
$$ E = 0 $$
La molécule \( BeCl_2 \) est de type \( AX_2 \) est de géométrie linéaire.
Planaire trigonale
Les molécules comportant trois paires d'électrons liés ont une forme plane trigonale. Pour te représenter cette forme, imagine un triangle équilatéral avec l'atome central de la molécule directement au milieu. Les trois paires d'électrons sont dirigées vers les trois coins du triangle. Si toutes les paires d'électrons sont des paires liées, l'angle entre elles est de \( 120^o \) .
Si une molécule comporte trois atomes, quelle serait la forme adoptée ? On suppose qu'avec trois atomes autour d'un atome central, les liaisons s'étaleraient autant que possible, ce qui donnerait une géométrie planaire trigonale (plan triangulaire).
Un exemple de molécule planaire trigonale est le trifluorure de bore, \( BF_3 \) .
Prenons la molécule \( BF_3 \) :
Autour de l'atome du bore \( B \) , se trouvent trois paires liées.
$$x= 3$$
$$E= 0$$
Alors cette molécule est de type \( AX_3 \) , elle est donc plane trigonale.
 Fig.5- Le trifluorure de bore, une molécule planaire trigonale.
Fig.5- Le trifluorure de bore, une molécule planaire trigonale.
Coudée
Plus tôt, nous avons appris que les paires d'électrons non liées repoussent les autres électrons plus fortement que les paires d'électrons liées. Si nous remplaçons l'une des paires d'électrons liés d'une molécule planaire trigonale par une paire d'électrons non liées, les deux liaisons restantes se resserrent, réduisant l'angle de liaison à un peu moins de \( 120° \) .
Cela forme une version d'une molécule planaire trigonale appelée molécule coudée.
Un exemple de molécule coudée est le dioxyde de soufre, \( SO_2 \) .
 Fig.6- Le dioxyde de soufre, une molécule coudée.
Fig.6- Le dioxyde de soufre, une molécule coudée.
Pour tes examens, tu dois seulement savoir que les paires d'électrons non liantes réduisent l'angle de liaison dans une molécule - tu n'as pas besoin de savoir le nombre exact de degrés dont la paire non liante réduit l'angle.
Théorie VSEPR sur les domaines à quatre électrons
Tétraèdre
Comment une molécule comportant quatre atomes autour d'un atome central se comporterait-elle en 3D ? Dans une représentation 2D, une molécule avec quatre domaines électroniques serait représentée avec des angles droits \( (90°) \) . Mais dans l'espace 3D, est-ce la répartition la plus optimale des paires d'électrons pour s'éviter ? Un angle de \( 90° \) permettrait-il une répulsion maximale entre les atomes liés ?
C'est ici qu'il faut sortir des sentiers battus. Une molécule à quatre domaines électroniques adopte une géométrie tétraédrique. Les angles de liaison sont de \( 109,5° \) , ce qui maximise un espace en 3D, plutôt qu'un simple plan. Imagine que les quatre domaines électroniques créent une certaine structure pyramidale.
Par exemple, le méthane, \( CH_4 \) , est constitué de quatre atomes d'hydrogène reliés à un atome de carbone central par des liaisons covalentes simples. Il s'agit d'une molécule tétraédrique dont les angles de liaison sont de \( 109,5° \) .
La molécule de méthane \( CH_4 \) est de type \( AX_4 \) .
 Fig.7 - méthane.2
Fig.7 - méthane.2
Mais comme pour les molécules planes trigonales, cette géométrie change légèrement lorsque nous remplaçons certaines des paires liantes par des paires non liantes :
- L'échange d'une paire liée contre une paire non liée diminue légèrement les angles de liaison restants et forme une molécule pyramidale trigonale, comme l'ammoniac.
- L'échange d'une deuxième paire de liaisons contre une paire non liée diminue encore plus l'angle de liaison restant et forme une molécule en forme de V, comme l'eau.
 Fig.8- Représentation des angles de liaison dans l'ammoniac et l'eau
Fig.8- Représentation des angles de liaison dans l'ammoniac et l'eau
La figure ci-dessous représente cette géométrie moléculaire et la répulsion des paires d'électrons qui crée une géométrie moléculaire tétraédrique.
 Fig.9- Tu peux voir comment une molécule avec quatre domaines électroniques étale ces domaines au maximum dans un espace 3D, créant une géométrie moléculaire tétraédrique avec des angles de liaison de 109,5°
Fig.9- Tu peux voir comment une molécule avec quatre domaines électroniques étale ces domaines au maximum dans un espace 3D, créant une géométrie moléculaire tétraédrique avec des angles de liaison de 109,5°
Note que l'angle de liaison de \( 109,5° \) d'une géométrie moléculaire tétraédrique n'est atteint que lorsque tous les domaines électroniques sont identiques, ce qui signifie que tous sont des paires d'électrons liées. Lorsqu'il y a un mélange de paires solitaires et de paires liées autour d'un atome central, les angles et par conséquent la forme changent. Cela est dû à la répulsion plus forte d'une paire d'électrons non liée par rapport à une paire liée.
Prends les exemples ci-dessous de \( NH_3 \) et \( H_2O \) , qui ont tous deux des paires libres autour d'un atome central.
Ici, les géométries moléculaires sont coudées pour l'eau, et sont pyramidales trigonales pour l'ammoniac.
Plane coudée
Dans \( H_2O \) , deux d'entre eux sont des paires solitaires, qui sont invisibles dans la géométrie moléculaire.
De plus, comme les paires non liées se repoussent davantage que les paires d'électrons liées, l'angle entre les liaisons se rapproche et devient inférieur à \( 109,5° \) , comme le prévoit la géométrie tétraédrique.
Pyramidale trigonale
Dans le cas de l'ammoniac \( (NH_3) \) , nous pouvons voir qu'il y a trois paires d'électrons liés, mais aussi une paire non liante. En prédisant les angles de liaison à partir de domaines à quatre électrons, nous pourrions affirmer que les angles de liaison seraient de \( 109,5° \) . Or, le couple solitaire repousse les liaisons, les rapprochant les unes des autres, créant ainsi l'angle de \( 107° \) que l'on observe dans les géométries pyramidales trigonales.
 Fig.10- Ammoniac est une molécule pyramidale trigonale.3
Fig.10- Ammoniac est une molécule pyramidale trigonale.3
Théorie VSEPR sur les domaines à cinq électrons
Bipyramide trigonale
Les molécules comportant cinq paires d'électrons sont basées sur une forme bipyramidale trigonale. Comme précédemment, nous allons commencer par examiner la forme formée lorsque toutes les paires d'électrons sont des paires liées. Trois des paires liées se disposent de manière similaire à une molécule plane trigonale : elles s'étalent de manière égale sur un plan à \( 120^o \) l'une par rapport à l'autre. Les deux autres paires liées se placent directement au-dessus et au-dessous de ce plan, à \( 90 ^o \) des trois autres liaisons.
Le pentachlorure de phosphore \( PCl_5 \) est un bon exemple de molécule bipyramidale trigonale. Il contient cinq atomes de chlore reliés à un atome de phosphore central par des liaisons covalentes simples.
 Fig.11- Le pentachlorure de phosphore est une molécule bipyramidale trigonale. 4
Fig.11- Le pentachlorure de phosphore est une molécule bipyramidale trigonale. 4
Une fois de plus, l'échange de certaines paires d'électrons liées contre des paires non liées modifie la forme de la molécule. Cela modifie également les angles de liaison restants.
- Une molécule comportant quatre paires d'électrons liés et une paire d'électrons non liées forme une molécule en balançoire. Le tétrafluorure de soufre en est un exemple.
- Une molécule avec trois paires de liaisons et deux paires non liées forme une molécule en forme de T. Le trifluorure de chlore \( ClF_3 \) en est un exemple.
- Une molécule avec seulement deux paires liées et trois paires non liées forme un autre type de molécule linéaire. Le difluorure de xénon \( XeF_2 \) en est un exemple.
Les domaines à cinq électrons créent une géométrie bipyramidale trigonale (bipyramidale triangulaire). Le terme "bipyramidale" signifie littéralement "deux pyramides". Il faut l'interpréter comme deux pyramides empilées l'une sur l'autre, les pyramides ayant une base triangulaire.
Théorie VSEPR sur les domaines à six électrons
Octaédrique
Une molécule avec six domaines d'électrons crée une géométrie octaédrique. Tu peux l'imaginer comme une forme à \( 8 \) côtés, comme un diamant - donc octaédrique, même s'il y a \( 6 \) atomes impliqués (et \( 6 \) sommets de la forme). Tu peux même y penser comme à deux pyramides empilées l'une sur l'autre, la base de la pyramide étant un carré. Les angles créés dans cette forme sont de \( 180 ^o \) et \( 90 ^ o \) .
Tu trouveras ci-dessous un exemple de la géométrie octaédrique VSEPR, représentée par une molécule de \( SF_6 \) . Tu peux voir comment les six atomes de fluor s'éloignent de l'atome de soufre central, créant ainsi une forme de "diamant" octaédrique en 3D.
Enfin, examinons les molécules comportant six paires d'électrons. Leur forme de base est l'octaèdre. Pour toi représenter une molécule octaédrique avec six paires de liaisons, imagine que l'atome central est placé directement au milieu d'un carré. Quatre des liaisons pointent vers les coins du carré ; elles sont toutes à \( 90 ^ o \) les unes des autres. Les deux autres paires d'électrons liés se trouvent directement au-dessus et au-dessous du plan. Cela signifie que ces liaisons sont également à \( 90 ^o \) par rapport à toutes les autres.
L'hexafluorure de soufre est un exemple courant de molécule octaédrique. Tous les angles entre ses liaisons simples \( S-F \) sont à \( 90° \) .
 Fig.12- L'hexafluorure de soufre est une molécule octaédrique. 6
Fig.12- L'hexafluorure de soufre est une molécule octaédrique. 6
L'échange de certaines paires d'électrons liées par des paires non liées modifie la géométrie de cette molécule et réduit l'angle entre les liaisons restantes.
- Le remplacement d'une paire liée par une paire isolée crée une molécule pyramidale carrée, comme le pentafluorure de brome.
- Le remplacement de deux paires de liaisons par deux paires non liées crée une molécule plane et carrée, comme le tétrafluorure de xénon.
 Fig. 13- Le tétrafluorure de xénon, une molécule plane et carrée.7
Fig. 13- Le tétrafluorure de xénon, une molécule plane et carrée.7
En utilisant les prédictions ci-dessus, tu peux voir comment la théorie VSEPR nous permet de tirer des conclusions concernant les formes 3D des molécules, en fonction de leurs domaines électroniques (paires d'électrons liés ou paires d'électrons solitaires).
Si tu as un modèle moléculaire en kit, essaie de fabriquer ces molécules et vois comment elles obéissent à la théorie VSEPR !
VSEPR : Exemple
Examinons quelques exemples de chaque forme prédite par la théorie VSEPR, et de cette façon, ils peuvent être appliqués à de nombreux contextes. Chacun des modèles théorisés sera pris en compte, et certains exemples courants seront montrés et discutés.
 Fig.14- Géométrie linéaire du dioxyde de carbone
Fig.14- Géométrie linéaire du dioxyde de carbone
 Fig.15 Géométrie trigonal planaire du trichlorure de bore
Fig.15 Géométrie trigonal planaire du trichlorure de bore
Ci-dessus, tu peux voir deux structures. L'une représente la molécule de \( CO_2 \) en tant qu'exemple de géométrie linéaire, tandis que l'autre montre une molécule de \( BCl_3 \) en tant qu'exemple de géométrie trigonale planaire, comme le prédit la théorie VSEPR. Les angles sont affichés. Ces structures sont confirmées expérimentalement, ce qui suggère que la théorie VSEPR est pertinente et tient la route dans des exemples concrets.
Ci-dessous, tu peux voir de quelle façon la géométrie tétraédrique prédite par la théorie VSEPR est représentée dans une molécule de méthane, \( CH_4 \) . Ici, les angles des liaisons forment l'angle prédit de \( 109,5° \) .
 Fig.7- VSEPR, géométrie tétraédrique du méthane.
Fig.7- VSEPR, géométrie tétraédrique du méthane.
Ce que tu peux voir ci-dessous est un exemple de la géométrie bipyramidale trigonale du \( PF_6 \) . Ici, tu peux clairement voir la différence entre la représentation 2D, une représentation de la structure de Lewis de la molécule, par rapport au modèle 3D. Les cinq domaines électroniques s'étalent aussi loin que possible en fonction de la répulsion des paires d'électrons pour créer la forme prédite - bipyramidale trigonale.
 Fig.16- Géométrie bipyramidale trigonale du pentafluorure de phosphore
Fig.16- Géométrie bipyramidale trigonale du pentafluorure de phosphore
Tu trouveras ci-dessous un exemple de la géométrie octaédrique VSEPR, représentée par une molécule de \( SF_6 \) . Tu peux voir de cette façon que les six atomes de fluor s'éloignent de l'atome de soufre central, créant ainsi une forme de "diamant" octaédrique en 3D.
 Fig.17- Géométrie octaédrique de l'hexafluorure de soufre
Fig.17- Géométrie octaédrique de l'hexafluorure de soufre
VSEPR : Tableau
À présent, tu devrais être familiarisé avec les formes des différentes molécules telles qu'elles sont dictées par la théorie VSEPR. Pour t'aider à consolider tes connaissances, nous avons créé un tableau pratique comparant les formes de base des molécules, leur nombre de paires d'électrons liés et leurs angles de liaison. Nous avons également inclus les noms des formes des variantes de ces molécules, qui apparaissent lorsque tu remplaces certaines des paires d'électrons liés par des paires non liées.
 Fig.18- Un tableau théorique VSEPR.
Fig.18- Un tableau théorique VSEPR.
C'est tout pour cette explication. Tu devrais maintenant savoir ce qu'est la théorie VSEPR et être capable de l'utiliser pour nommer, identifier et dessiner les formes de molécules comportant entre deux et six paires d'électrons liés. Tu devrais également être en mesure d'expliquer l'effet des paires d'électrons non liées sur la géométrie des molécules.
VSPER - Points clés
- La théorie VSEPR est un ensemble de règles utilisées en chimie pour prédire la géométrie d'une molécule. Elle est basée sur le nombre et la disposition des électrons de valence de la molécule.
- La théorie VSEPR repose sur deux principes clés :
Les paires d'électrons se repoussent mutuellement. Pour cette raison, elles essaient de se positionner le plus loin possible les unes des autres, ce qui donne aux molécules ayant le même nombre de paires d'électrons la même forme de base.
Les paires d'électrons isolées repoussent davantage les autres électrons que les paires liées. De ce fait, elles réduisent l'angle de liaison dans les molécules, ce qui modifie légèrement la forme de la molécule.
Les molécules avec deux paires d'électrons sont basées sur des molécules linéaires avec un angle de liaison de \( 180^o \) .
Les molécules avec trois paires d'électrons sont basées sur des molécules planes trigonales avec un angle de liaison de \( 120^o \) .
Celles avec quatre paires d'électrons sont basées sur des molécules tétraédriques avec un angle de liaison de \( 109,5^o \) .
Les molécules à cinq paires d'électrons sont basées sur des molécules bipyramidales trigonales. Elles ont des angles de liaison de \( 90^o \) et \( 120^o \) .
Enfin, les molécules à six paires d'électrons sont basées sur des molécules octaédriques dont l'angle de liaison est de \( 90^o \) .
References
- Expii
- commons.wikimedia.org
- commons.wikimedia.org
- commons.wikimedia.org
- commons.wikimedia.org
- commons.wikimedia.org
Sujets similaires dans Physique-chimie


























